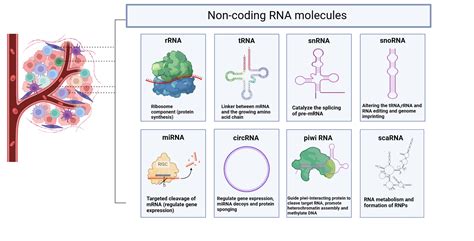
Úvod do izolácie DNA
Izolácia nukleových kyselín je prvým krokom v mnohých experimentoch molekulárnej biológie. Ideálne je potrebné získať cieľovú nukleovú kyselinu (DNA alebo RNA) v dostatočnom množstve a kvalite, to je bez prímesí „nadbytočných” látok, tzv. kontaminantov. V biológii je nevyhnutné izolovať čistú, vysokomolekulárnu DNA, pričom postačujúca je fragmentovaná DNA s dĺžkou fragmentov 70-150 kb.
Nukleové kyseliny je možné izolovať z rôznych zdrojov. DNA možno teoreticky izolovať z akejkoľvek živočíšnej tkáne obsahujúcej živé bunky. U organizmov malej veľkosti sa k izolácii používa aj celých jedincov. DNA môže byť izolovaná aj z extrémnych zdrojov ako je pôda, úžitková voda, potraviny a iné. Pre izoláciu sa používa celá rada rôznych protokolov a v poslednej dobe sa tiež často používajú komerčne vyrábané súpravy (kity), ktoré však bývajú drahšie.
Voľba metódy extrakcie DNA závisí od toho, k čomu ju budeme ďalej používať. Napríklad, pri použití metódy PCR (polymerázová reťazová reakcia) postačujú malé množstvá DNA, ktorej čistota a integrita nie sú vo väčšine prípadov kritické. Na druhej strane, pri klonovaní, enzymatickom opracovaní DNA restrikčnými endonukleázami alebo pri sekvenovaní sú potrebné relatívne väčšie množstvá DNA s vyššou čistotou. S kvalitne izolovanou DNA sa nám však vždy bude pracovať lepšie.
Špecifiká izolácie DNA z fosílnych a náročných vzoriek
Často možno izolovať DNA aj z múzejného materiálu. Dobrým zdrojom DNA sú hlavne tkanivá uchovávané v liehu. DNA bola úspešne izolovaná z fosílnych kostí (napríklad z neandrtálca) alebo z hmyzu uchovaného v jantáre. Väčšiu nádej na úspech možno očakávať v prípade, že kosť bola dlhú dobu v chladnom prostredí (napríklad v permafroste).
Pri takýchto izoláciách je však potrebné postupovať veľmi opatrne a starostlivo, pretože riziko kontaminácie je veľké. Používajú sa špeciálne pretlakové miestnosti v budovách, kde nie sú žiadne ďalšie molekulárne laboratóriá a pracovníci používajú špeciálne obleky pripomínajúce skafandre, aby maximálne obmedzili kontamináciu vzorky svojou vlastnou DNA. Naopak, izolácia DNA zo vzoriek, ktoré prišli do styku s formalínom, často končí neúspechom. Pri izolácii tkanív uchovávaných vo formalíne sa v prvých krokoch izolácie niekedy pridáva DTT (až v 100 mM koncentrácii) alebo sa využívajú špeciálne kity.

Kroky izolácie DNA: od lýzy po purifikáciu
Príprava vzorky a lýza buniek
Na izoláciu DNA je dôležité dôkladné rozrušenie pletív buniek a ich súčastí. Aby došlo k uvoľneniu nukleovej kyseliny do vodného roztoku, je potrebné rozrušiť (dezintegrovať) bunkové steny a biomembrány. Bunky sa obvykle rozrušujú v prostredí príslušného extrakčného činidla, ktoré má overenú iónovú silu, reakciu prostredia a obsahuje inhibítory nukleáz.
V prípade, že sa bunková kultúra pestuje v tekutom médiu, je prvým krokom izolácie oddelenie buniek od média centrifugáciou. Pre izoláciu z buniek (napr. z čiastočky tkaniva, buniek bukálnej sliznice získaných sterom, leukocytov periférnej krvi) je obvykle prvým krokom homogenizácia tkaniva a lýza buniek.
Možno povedať, že bunky vyšších organizmov sa deštruujú ľahšie a jednoduchšie, naopak rastlinné bunky a pletivá, ako aj bunky mikroorganizmov sú rezistentnejšie. Ich rozbíjaním sa môžu niekedy poškodiť i štruktúry niektorých druhov nukleových kyselín. Vo všeobecnosti sa ťažšie izolujú nukleové kyseliny z rastlinných buniek kvôli prítomnosti kompaktnej celulózovej bunkovej steny a chemických zlúčenín obsiahnutých vo vakuolárnej šťave.
Jedným z najviac používaných postupov deštrukcie rastlinných buniek a pletív je mechanické rozdrvenie materiálu, ktoré však niekedy môže zapríčiniť i čiastočnú degradáciu nukleových kyselín. Výhodnejším môže byť zmrazenie rastlinného materiálu v kvapalnom dusíku s nasledujúcim rozdrvením na prášok a extrakciou v mixéri alebo v sklenenom homogenizátore. Na uvoľnenie obsahu rastlinných buniek obalených bunkovou stenou sa používa v prvom kroku mechanické, ako aj enzymatické opracovanie (celulázy). Extrakt z mimoriadne ťažko deštruujúceho materiálu možno získať tak, že sa pletivo najprv odvodní v 95% etanole alebo etylénglykole a extrakt sa potom postupne premýva etanolom, etanolom - etyléterom v pomere 3:1, etanolom - etyléterom v pomere 1:1, bezvodným etyéterom a nakoniec sa dosuší v prúde dusíka.

V prípade niektorých baktérií, ktoré majú veľmi hrubú bunkovú stenu alebo tvoria veľa sekundárnych metabolitov, je výhodné izolovať DNA z buniek v logaritmickej fáze rastu, t.j. pri ich aktívnom hromadnom delení. Na lýzu bakteriálnych buniek sa najčastejšie používa enzymatické opracovanie bunkovej steny lyzozýmom, ktorý hydrolyzuje glykozidické väzby v peptidoglykánoch. Druhým krokom je rozrušenie cytoplazmatickej membrány bakteriálnej bunky pôsobením ionogénnych detergentov (detergentov tvoriacich ióny), napr. SDS − dodecylsulfát sodný. Nevzácne je treba okrem chemickej lýzy použiť aj mechanickú lýzu bakteriálnych buniek pomocou ultrasonikátora, ktorý na disrupciu buniek využíva ultrazvukové vlny.
V prípade izolácie nukleových kyselín zo živočíšnych tkanív a celých orgánov (myšacia slezina, pečeň, mozog) je potrebná homogenizácia vstupného materiálu. K tomuto účelu je možné použiť mechanické rozdrvenie v homogenizátore alebo rozrušenie bunkovej hmoty zmrazením v tekutom dusíku. Živočíšne bunky sú obalené len cytoplazmatickou membránou, a preto je možné dosiahnuť ich lýzu jemnejšími prostriedkami, napr. pôsobením slabých neionogénnych detergentov (napr. Triton X-100) v kombinácii s proteolytickými enzýmami, ako je proteináza K.
Bunkové a jadrové membrány sa obvykle rozpúšťajú účinkom tenzidov. K rozpadu bunkových štruktúr prispieva degradácia proteínov pomocou enzýmov proteáz, napr. proteinázy K. Dôležitým faktorom je aj prítomnosť chelatačných činidiel (napr. EDTA − kyselina etyléndiamíntetraoctová), ktoré z roztoku „vychytávajú” dvojmocné katióny (Mg²⁺, Ca²⁺), čím inaktivujú bunkové DNázy. Neprítomnosť dvojmocných katiónov zároveň destabilizuje vonkajšiu bakteriálnu membránu.
Pri lýze sa uvoľní celý obsah buniek do roztoku, pričom vznikne komplexná zmes obsahujúca zvyšky bunkových stien a bunkových membrán, proteíny, nukleové kyseliny, polysacharidy a rôzne nízkomolekulové zložky (obzvlášť dôležité pri izolácii z rastlinných buniek kvôli prítomnosti chemických zlúčenín vakuolárnej šťavy). Aby nedochádzalo k degradácii izolovanej nukleovej kyseliny je potrebné použiť čo najmiernejšie podmienky lýzy, t.j. uskutočňovať ju v tlmivom roztoku a v chlade.
Odstránenie kontaminujúcich látok
Princípom purifikácie akéhokoľvek materiálu z buniek je cieľom zbaviť sa zložiek, ktoré pri ďalšej práci nepotrebujeme. Pri izolácii nukleových kyselín je dôležité odstrániť zo zmesi proteíny, medzi ktoré patria aj bunkové nukleázy, ktoré môžu degradovať izolovanú nukleovú kyselinu, ako aj proteíny viažúce sa na DNA, ktoré svojou prítomnosťou môžu rušiť následné analýzy (napr. štiepenie restrikčnými endonukleázami). Dôkladné prečistenie preparátov nukleových kyselín od bielkovinových prímesí sa dá uskutočniť viacerými postupmi, v ktorých použité činidlá denaturujú prítomné bielkoviny a nukleové kyseliny zostávajú rozpustené vo vodnej fáze bez toho, aby sa porušila ich štruktúra.
Na odstránenie proteínov z preparátov nukleových kyselín sa často používa extrakcia organickými rozpúšťadlami, najčastejšie zmesou fenolu a chloroformu (trichlórmetánu). Tieto látky sú s vodou nemiešateľné, a preto sa po ich pridaní k vodnému roztoku nukleových kyselín vytvoria dve fázy. Pri premiešaní takejto zmesi dochádza na fázovom rozhraní k denaturácii proteínov. Ak sa roztok nukleových kyselín extrahuje fenolom s neutrálnym pH, nukleové kyseliny zostávajú po extrakcii vo vodnej fáze. Fenol-chloroformová metóda je najpoužívanejšou technikou organickej extrakcie DNA. Hoci je náročnejšia na čas a pracuje sa pri nej s nebezpečnými chemikáliami, umožňuje dosiahnuť vysokých výťažkov a získať prakticky čistú DNA. Medzi výhody organickej extrakcie patrí vysoký výťažok a vysoká čistota purifikovanej DNA. Fenol-chloroformová technika je preto stále „zlatým štandardom“ purifikácie nukleových kyselín.
Extrakce DNA - vylepšená metoda fenol:chloroform
Po fenolovej extrakcii je dôležité zbaviť roztoky nukleových kyselín zvyškov fenolu, pretože fenol môže inhibovať následné enzymatické reakcie (napr. restrikčné štiepenie). Z deproteinizačných prostriedkov sa na izoláciu nukleových kyselín používajú najčastejšie fenol, chloroform, guanidínchlorid a chloristan sodný. Vo väčšine prípadov však spoľahlivo funguje klasická metóda založená na odstránení proteínov pomocou enzýmu proteinázy K, extrakcie zmesí fenolu s chloroformom a precipitácii čistým liehom. Proteináza K je účinný bakteriálny enzým, ktorý má teplotné optimum okolo 60 °C, nevyžaduje vápenaté ani horečnaté ióny a nie je inhibovaný ani koncentrovanými tenzidmi. Čiastočne hydrolyzuje kontaminujúce bielkoviny. Nasleduje denaturácia bielkovín a ich vyzrážanie zmesou fenolu a chloroformu. Fenol-chloroformová zmes sa nemieša s vodou. Pri pH roztoku nad 7,6 je DNA disociovaná a zostáva rozpustená vo vodnej fáze, zatiaľ čo proteíny sa denaturujú a vypadávajú do hydrofóbnej fázy. Ku zmesi sa pridáva malé množstvo izoamylalkoholu, ktorý uľahčí oddelenie fáz a zabráni peneniu pri spracovávaní vzoriek bohatých na proteíny.
Na odstránenie RNA z preparátov DNA sa používa pankreatická RNáza. Tento enzým je veľmi stabilný a zároveň nevyžaduje pre svoju aktivitu dvojmocné ióny, čo neplatí napríklad pre DNázy. Enzymaticky sa DNA od RNA očisťuje pomocou špecifických ribonukleáz, ktoré degradujú RNA na oligoribonukleotidy. Deproteinovaný bunkový extrakt sa nechá inkubovať 30 minút pri 37 °C v prítomnosti pankreatickej ribonukleázy, z ktorej sa musia pred samotným použitím odstrániť stopy deoxyribonukleázy. 0,2 % roztok kryštalickej pankreatickej ribonukleázy v 0,15 mol.dm-3 roztoku chloridu sodného s pH 5,0 sa predinkubuje 10 minút pri 80 °C. Preparát DNA sa po inkubácii s enzýmom precipituje etanolom, kým hydrolyticky uvoľnené oligoribonukleotidy zostávajú v roztoku.
Preparáty nukleových kyselín pripravené základnými izolačnými postupmi obvykle nepredstavujú homogénne populácie. Nejde tu len o zmesi jednotlivých druhov nukleových kyselín, ale často aj o prímes iných interferujúcich látok, najmä polysacharidov a ďalších fosfátových esterov. Oddelenie nukleových kyselín a polysacharidov možno urobiť pomocou cetyltrimetylamoniumbromidu (CTA). Pomocou neho možno oddeliť oba druhy nukleových kyselín, pričom polysacharidy a väčšina ďalších fosfátových esterov zostáva v roztoku. CTA - soli nukleových kyselín sa odcentrifugujú, opakovane sa premyjú 70% etanolom a etyléterom a nakoniec sa dosušia vo vákuu.
Koncentrácia a finálna purifikácia DNA
Na prečistenie nukleových kyselín od nízkomolekulových látok (soli, zvyšky fenolu) a na skoncentrovanie vzorky sa používa alkoholové zrážanie (najčastejšie čistým, bezvodým etanolom alebo izopropanolom). Po odstránení kontaminujúcich bielkovín a lipidov je DNA stále znečistená prevažne nízkomolekulárnymi látkami. Následuje preto vyzrážanie DNA z roztoku napríklad jej vysolením alebo pomocou jednoduchých alkoholov (etanolu alebo izopropanolu). Zrážanie sa robí v prítomnosti jednomocných iónov (napr. 0,1 M octan sodný) a pri nízkej teplote (-20 °C). V týchto podmienkach je výťažok kvantitatívny aj pri nízkej koncentrácii DNA. Na druhej strane, zrážanie pri laboratórnej teplote (+20 °C) je výhodné, ak chceme vyzrážať DNA bez súčasného vyzrážania („oživenia”) kontaminujúcej RNA. Vysrážaná nukleová kyselina sa nazýva precipitát.
Precipitát DNA sa od roztoku oddelí vysokootáčkovou centrifugáciou. Premytím 70 % etanolom sa odstránia zvyšky solí prítomné v precipitáte a precipitát sa vysuší tak, aby sa odparili zvyšky etanolu, ale zároveň aby DNA zostala hydratovaná. Následne sa DNA vyzráža z vodného roztoku. Najprv sa pridá vo veľkej koncentrácii vhodná soľ (chlorid sodný, octan sodný a pod.). Jej ióny si vytvárajú hydratačný obal, čím odoberú DNA rozpúšťadlo (tzv. vysoľovanie). Potom sa ku zmesi pridá málo polárna látka (napríklad etanol).
DNA môže byť purifikovaná zo zmesi makromolekúl ultracentrifugáciou za pomoci chloridu cézneho (CsCl) a etídium bromidu. DNA sa skoncentruje do úzkeho prúžku v strede gradientu, pričom lineárna a cirkulárna (plazmidová) DNA majú inú hustotu, a preto je možné ich touto metódou navzájom oddeliť. Po centrifugácii sa vyberú frakcie obsahujúce DNA, etídium bromid sa odstráni extrakciou n-butanolom a DNA sa z roztoku získa etanolovou precipitáciou. Výsledkom tejto techniky je vysokomolekulárna DNA s vysokou čistotou.
Ďalšie metódy extrakcie DNA sú založené napríklad na využití kremičitých guličiek s veľkým povrchom, ktorými je napríklad naplnená krátka chromatografická kolónka. Vo vodných roztokoch je povrch silikátu hydratovaný. Prídavkom vysokej koncentrácie tzv. chaotropných solí pri vhodnom pH dôjde k rozbitiu vodíkových mostíkov medzi molekulami vody a povrchom silikátu. Na takto dehydrovaný silikát sa svojimi fosfátovými skupinami s vysokou afinitou viaže DNA. Kontaminujúce látky je potom možné odmyť. Extrakcia pomocou silikátovej pevnej fázy je relatívne jednoduchá a hodí sa aj pre automatizáciu.
Pri magnetickej separácii sa DNA reverzibilne viaže na magnetické guličky potiahnuté vhodným povrchom - protilátkami proti DNA, silikátom, iónomeničom alebo povrchom s inými vhodnými funkčnými skupinami. Po naviazaní DNA sa guličky pomocou magnetu oddelia od roztoku s kontaminujúcimi látkami a opakovane sa premyjú. Magnetická separácia je vhodná k automatizácii a používa sa predovšetkým pre spracovanie veľkého počtu vzoriek. Výťažky a čistota DNA sú porovnateľné so silikátovou extrakciou, je však možné izolovanú DNA získať v menšom množstve roztoku (t.j. koncentrovanejšiu).
Analýza kvality a skladovanie DNA
Koncentráciu izolovanej DNA určíme spektrofotometrom alebo pomocou elektroforézy v málo koncentrovanom agarózovom géli a porovnaním so štandardmi, ktoré nanesieme na gél spoločne so študovaným vzorkom. Izolovanú DNA pred použitím obvykle zriedime vodou a zásobní koncentrovaný roztok uchováme v mrazničke. Molekula DNA v kyslom prostredí môže spontánne degradovať, a preto sa DNA rozpúšťa v slabo zásaditom tlmivom roztoku s prídavkom EDTA (tzv. roztok TE).
Riešenie bežných problémov pri izolácii DNA
Fragmentácia DNA
Príčina: Nadmerná homogenizácia/vortexovanie vzorky.
Riešenie: Nevortexovať vzorky DNA, nepoužívať mechanické narušenie tkanív. Jemne homogenizovať pipetovaním.
DNA kontaminovaná Dnázami
Príčina: Prítomnosť aktívnych Dnáz.
Riešenie: Používať rukavice pri izolácii DNA a pracovať čo najčistejšie (používať reagencie, ktoré boli otestované na prítomnosť Dnáz).
Nízky výťažok DNA
Príčina: Tkanivo obsahuje oveľa nižšie hladiny NK ako sa očakávalo.
Riešenie: Zvýšiť množstvo tkaniva/buniek, ktoré má byť homogenizované.
Príčina: Neúplná lýza buniek.
Riešenie: Úplné rozsuspendovanie buniek, predĺžiť čas potrebný na lýzu buniek.
Príčina: Neúplná elúcia.
Riešenie: Väčší elučný objem a dlhšia doba elúcie môže zvýšiť výťažok.
Príčina: Neúplná obnova vyzrážanej DNA.
Riešenie: Po zrážaní a centrifugácii môžu byť časti DNA prilepené na stene mikroskúmavky.
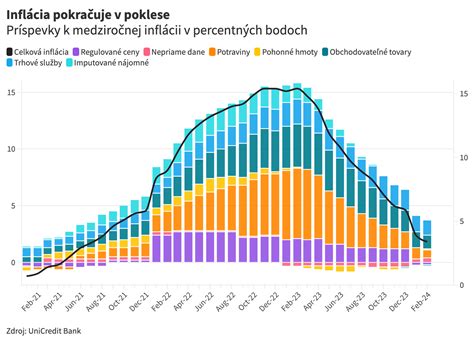
Izolácia RNA: Špecifiká a výzvy
Pri izolácii RNA z akéhokoľvek biologického materiálu je hlavným problémom jej nestabilita. Molekula RNA podlieha degradácii oveľa ľahšie ako DNA a zároveň ribonukleázy sú vo všeobecnosti veľmi stabilné a všadeprítomné enzýmy, ktoré nepotrebujú k svojej aktivite ako kofaktory dvojmocné ióny, na rozdiel od DNáz. Vedeli ste, že...? RNáza sa skutočne vyskytuje všade. Vylučuje sa aj potnými žľazami na končekoch prstov, takže práca bez rukavíc je absolútne neprípustná.
Metódy izolácie a purifikácie RNA sú založené na rýchlej lýze buniek, ktorá efektívne neutralizuje prítomné nukleázy. Kontaminujúce bielkoviny sa odstraňujú fenolovou extrakciou v kyslom prostredí alebo na silikagélových kolónkach. Zvyšky chromozomálnej DNA je možné rozložiť pôsobením DNázy. Purifikovaná RNA sa využíva na prípravu komplementárnej DNA (cDNA), northernovu hybridizáciu, RT-PCR, alebo na in vitro transláciu.
Pri mnohých aplikáciách je výhodné použiť iba frakciu mRNA. V princípe, izolácia mRNA spočíva vo využití prirodzenej enzymatickej posttranskripčnej modifikácie eukaryotickej mRNA, a to je pridávanie poly(A)-chvostíka na 3'-koniec molekuly mRNA za pomoci enzýmu poly(A)-polymerázy. Oligo-dT nosiče sú jednoduché plôšky, na ktorých sú fixované jednovláknové molekuly so sekvenciou poly(T), a teda sú komplementárne k jednovláknovým mRNA s poly(A) koncami. Ak sa roztok s prítomnými mRNA naleje na tieto nosiče, v prostredí s vyššou iónovou silou (pridanie solí) dochádza k hybridizácii, a teda zachytávaniu mRNA na týchto nosičoch.