Obezita, definovaná ako nadbytok telesného tuku v prirodzenej telesnej hmote, je spätá s vážnymi psychologickými a zdravotnými ťažkosťami ako je hypertenzia, zvýšená hladina tukov v krvi, diabetes mellitus typ II alebo diabetes mellitus nezávislý na inzulíne (NIDDM).
Asimilácia, uchovanie a využitie energie zo živín je súčasťou komplexného vnútorného systému, veľmi dôležitého pre existenciu mnohobunkových živočíchov. Pre suchozemské cicavce sú veľké zásoby metabolického paliva, napr. triglyceridov, v tukových tkanivách kritické pre prekonanie obdobia bez potravy. Nutnosť udržiavať energetické zásoby na stálej hladine, bez toho, aby priebežne dochádzalo k zmenám veľkosti a tvaru tela, vyžaduje rovnováhu medzi príjmom a výdajom energie. Mechanizmy regulácie energetickej rovnováhy na molekulárnej úrovni je však nutné najprv objasniť. Izolácia molekúl, ktoré vedú nutričné informácie a ovplyvňujú energetickú rovnováhu, bude kľúčom k pochopeniu regulácie telesnej hmotnosti zdravého aj chorého organizmu.
Individuálna hladina adipozity je do značnej miery daná geneticky. Sledovanie miery zhody v telesnej hmotnosti a adipozite medzi mono- a dizygotnými dvojčatami, adoptívnymi deťmi a ich biologickými rodičmi ukázalo, že dedičnosť obezity (0,4-0,8) prevyšuje dedičnosť mnohých iných vlastností zvyčajne považovaných za dedičné, ako je schizofrénia, alkoholizmus a ateroskleróza.
Podobnosti z hľadiska miery výdajov energie medzi príbuznými boli tiež opísané. Genetická analýza geograficky ohraničených populácií naznačila, že relatívne malý počet génov je príčinou 30-50 % odlišnosti v telesnej stavbe.
Na hlodavčích obezitných modeloch bolo nájdených sedem zrejmých mutácií v jednom géne. Najlepšie sú preštudované mutácie na myších obezitných modeloch v génoch OB (obezity) a DB (diabetes). Pokiaľ nie sú OB a DB prítomné v geneticky rovnakom druhu, je výsledkom metabolický a behaviorálne nerozlíšiteľný fenotyp, čo označuje, že tieto gény pôsobia rovnakou fyziologickou cestou. Homozygótne myši od oboch mutácií sú hyperalergické a hypometabolické a vyvinú obézny fenotyp zrejmý už vo veku jedného mesiaca. Ich hmotnosť sa stabilizuje na 60 až 70 g (oproti 30 až 35 g kontrolných myší).
OB a DB zvieratá manifestujú mnohé ďalšie hormonálne a metabolické zmeny, ktoré sťažujú rozpoznanie primárnej poruchy vyvolanej mutáciou.
Na všetkých hlodavčích obezitných modeloch boli pozorované zmeny v metabolizme uhľovodíkov pripomínajúce ľudský diabetes typ II. V niektorých prípadoch závisí stupeň diabetu z časti na histórii myšieho kmeňa. Ako OB tak aj DB kongénne C57B1/Ks myši vyvinuli ťažký diabetes s konečnou nekrózou β buniek a atrofiou ostrovčekov vedúcou k relatívnej inzulínopenii. Naproti tomu OB aj DB kongénne C57B1/6J myši vyvinuli prechodný inzulín-rezistentný diabetes, ktorý môže byť kompenzovaný hypertrofiou β buniek pripomínajúcou ľudský diabetes typ II.
Fenotyp OB a DB myší pripomína ľudskú obezitu inak než rozvinutý diabetes - mutantné myši prijímajú viac potravy a vydávajú menej energie ako chudé kontrolné myši (podobne ako obézni ľudia). Tento fenotyp tiež pripomína zvieratá s porušeným ventromediálnym hypotalamom, čo naznačuje, že obidve mutácie interferujú so schopnosťou správne prijímať alebo reagovať na nutričné informácie v rámci centrálneho nervového systému. Túto hypotézu podporujú aj výsledky parabiotických experimentov, podľa ktorých OB myši majú nedostatočný cirkulujúci faktor pocitu sýtosti a DB myši sú rezistentné voči účinkom OB faktoru (pravdepodobne vďaka defektu OB receptoru). Z experimentov vyplýva, že obezita mutantných myší môže viesť k rôznym defektom v aferentnej kľučke a/alebo integračnom centre predpokladaného spätnoväzobného mechanizmu regulujúceho stavbu tela.
Gény OB a DB sa nachádzajú na počiatku chromozómu 6 respektíve v polovici chromozómu 4. V obidvoch prípadoch zasahujú mutácie oblasti myšieho genómu zhodné s ľudskými, čo znamená, že pokiaľ existujú ľudské homológy OB-a DB, pravdepodobne budú mutácie zasahovať ľudské chromozómy 7q respektíve 1p. Defekty OB génu vedú k obezite aj u ďalších druhov cicavcov: u geneticky krížených krýs Zucker FA/FA s Brown Norway +/+ je FA mutácia (krysí chromozóm 5) napadnutá v rovnakom mieste ako u DB myší.
Vzhľadom na mnoho faktorov, ktoré môžu ovplyvňovať telesnú hmotnosť, nebolo možné predvídať, ktoré faktory a najmä ktoré homeostatické mechanizmy primárne určujú telesnú hmotnosť. Základným predmetom predkladaného vynálezu sú teda modulátory telesnej hmotnosti so schopnosťou regulovať adipozitu a obsah tukov u cicavcov.
Podľa predkladaného vynálezu je problém regulácie adipozity a obsahu tukov u zvierat, najmä cicavcov, riešený na úrovni obezitných (OB) polypeptidov a nukleových kyselín, ktoré tieto peptidy kódujú. Predkladaný vynález poskytuje najmä izolované polypeptidy schopné modulovať, t.j. kontrolovať a regulovať, telesnú hmotnosť a adipozitu. Predkladaný vynález taktiež prináša sekvencie nukleových kyselín kódujúcich tieto polypeptidy, čo umožňuje rekombinantnú produkciu OB polypeptidov a použitie samotných nukleových kyselín ako modulátorov telesnej hmotnosti.
OB polypeptidy patria aj ich alelické varianty alebo analógy vrátane fragmentov, ktoré majú rovnakú biologickú aktivitu. OB polypeptidy možno pripraviť rekombinantnými alebo chemickými postupmi. Výhodné predkladané OB polypeptidy sú polypeptidy s aminokyselinovou sekvenciou SEQ ID č. 2, 4, 5 alebo 6 a ich alelické varianty alebo analógy vrátane fragmentov.
Imunogénne fragmenty OB polypeptidov predkladaného vynálezu zahŕňajú: Val-Pro-Ile-Gln-Lys-Val-Gln-Asp-Asp-ThrLys-Thr-Leu-Ile-Lys-Thr (SEQ ID č. 18); Leu-ľii s-Pro-I le-LeuSer-Leu-Ser-Lys-Met-Asp-Gln-Thr-Leu-Ala (SEQ ID č.19); SerLys-Ser-Cys-Ser-Leu-Pro-Gln-Thr-Ser-Gly-Leu-Gln-Lys-Pro-GluSer-Leu-Asp (SEQ ID č.20); a Ser-Arq-Leu-Gln-Gly-Ser-LeuGln-Asp-Ile-Leu-Gln-Gln-Leu-Asp-Val-Ser-Pro-Glu-Cys (SEQ ID č.21).
Ľudské analógy OB polypeptidov majú aminokyselinovú sekvenciu zodpovedajúcu SEQ ID č.4 a 6, v ktorých je jedna alebo niekoľko aminokyselín z aminokyselín 53, 56, 71, 85, 89, 92, 95, 98, 110, 118, 121, 122, 126, 127, 128, 129, 132, 139, 157, 159, 163 a 166 (číslované podľa SEQ ID č.4) substituovaných inými aminokyselinami, napríklad divergentnými aminokyselinami myšieho OB polypeptidu SEQ ID č.2 alebo alanínom. Ľudské analógy OB polypeptidov zahŕňajú polypeptidy, v ktorých je:
- jeden alebo niekoľko zvyškov kys. aspartovej substituovaných kys. glutámovou;
- serín v polohe 98 substituovaný glycínom, alanínom, valínom, cysteínom metionínom alebo treonínom; a
- arginín v polohe 92 substituovaný asparagínom, lyzínom, histidínom, glutamínom, kys. glutámovou, aspartovou, serínom, treonínom, metionínom alebo cysteínom.
Analóg OB polypeptidu predkladaného vynálezu je výhodne z 83% alebo viac sekvenčne homológový so sekvenciou ľudského OB polypeptidu SEQ ID č.2, 4, 5 alebo 6.
Purifikácia heterogénneho proteínu
Purifikácia nadexprimovaného proteínu tvorí druhú, a nemenej dôležitú, fázu produkcie čistého rekombinantného proteínu v heterologickom expresnom systéme. Málokedy získavame rekombinantný proteín priamo z tekutého, mimobunkového (extracelulárneho) prostredia (kultivačného média), hoci niektoré expresné systémy takúto sekréciu proteínov umožňujú.
Prvým krokom k purifikácii akejkoľvek molekuly z biologického materiálu je rozrušenie bunkovej steny a cytoplazmatickej membrány, čím dôjde k jej uvoľneniu do roztoku.
Metódy disrupcie buniek
Poznáme niekoľko spôsobov disrupcie buniek:
- opakované zamrazenie a rozmrazenie materiálu - disrupciu spôsobia tvoriace sa ľadové kryštáliky (môže denaturovať niektoré proteíny)
- mechanické - homogenizácia v trecej miske alebo zložitejších aparatúrach
- chemické - rôzne silné detergenty, rozpúšťadlá (môžu denaturovať niektoré proteíny; nutné použiť pri solubilizácii membránových proteínov − napr. Triton X-100, CHAPS)
- enzymatické - pôsobenie enzýmov na bunkové steny (napr. celulázy, pektinázy, lyzozým pre baktérie, zymoláza pre kvasinky)
V prípade proteínov závisí od ich lokalizácie (napr. bunkové jadro, cytoplazma, membránový proteín, periplazmatická lokalizácia v prípade gram-negatívnych baktérií) ako aj od pôvodu a charakteru buniek (prítomnosť bunkovej steny), akú „agresívnu” metódu (príp. kombináciu metód) musíme použiť, aby sme:
- uvoľnili dostatočné množstvo proteínu do roztoku, t.j. rozpustnej (solubilnej) fázy
- zachovali tvar (konformáciu) a biologickú aktivitu proteínu
Po uvoľnení proteínov do roztoku treba zamedziť pôsobeniu enzýmov - proteáz, ktoré by tieto „nechránené” proteíny mohli samovoľne degradovať. Preto sú dôležitou zložkou každého roztoku inhibítory proteáz. Na druhej strane, môžu sa hodiť enzýmy, ktoré degradujú napr. nukleové kyseliny - nukleázy (DNázy a RNázy, príp.

Homogenizácia
Homogenizácia patrí medzi mechanické spôsoby disrupcie buniek. Po homogenizácii sa dostanú proteíny do roztoku, ktorý musí mať určité primerané zloženie a pH, aby nedošlo k strate ich biologických vlastností.
| Pufor | Rozsah pH |
|---|---|
| Fosfátový (NaH₂PO₄ + Na₂HPO₄) | 5,8 − 8,0 |
| Tris-HCl | 7,0 − 9,0 |
| Citrátový (octan sodný + kys. | - |
Zdroj: EMBL, Protein PurificationExtraction and Clarification
Najpoužívanejšími homogenizátormi sú:
- Potterov homogenizátor - materiálom sú najčastejšie bunkové kultúry živočíšneho pôvodu, ktoré sa homogenizujú trením piestu o sklenený mažiar v tvare valca
- ultrazvukový homogenizátor, tzv.
Použitie rôznych chemických látok ako prímesí (aditív) tlmivého roztoku nie je vždy nevyhnutné. Sú to látky, ktoré pomáhajú solubilizovať alebo stabilizovať niektoré proteíny. Vhodne zvolené aditíva by nemali ovplyvňovať ďalšie purifikačné procedúry, príp.
Centrifugácia
Homogenát obsahuje rôzne veľké a ťažké častice (bunkový debris, t.j. zvyšky buniek, organel, membrán) a rozpustný (solubilný) materiál. Použitím viacerých cyklov centrifugácie s odlišnými rýchlosťami a časom vieme do istej miery separovať určité frakcie so želanými proteínmi. Centrifugácia pri veľmi nízkych otáčkach (500 g / 10 min) umožňuje izolovať najťažšie bunkové jadrá), takže sa hodí na extrakciu jadrových proteínov. Ak predpokladáme, že náš rekombinantný proteín je solubilný, centrifugujeme pri vyšších otáčkach (10 000 g / 20 min), čím sa zbavíme väčšiny nepotrebného, kontaminujúceho materiálu. Naproti tomu, izolácia membránových častíc s membránovými proteínmi vyžaduje ultracentrifugáciu (100 000 g / 60 min).
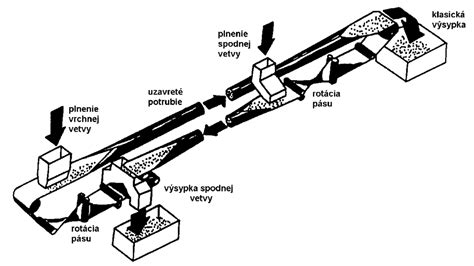
Centrifugácia rozdeľuje suspenziu na nerozpustný sediment (pelet) (na dne skúmavky) a supernatant (roztok).
Niekedy sa však môže hodiť diferenciálna centrifugácia v hustotnom gradiente (napr. sacharózy), najmä ak chceme od bunkového debrisu oddeliť bunkové organely alebo ľahšie inklúzne telieska, tvorené agregátmi rekombinantného proteínu. V tom prípade sa najťažší debris usadí v spodnej časti skúmavky, ale ľahšie častice nevedia klesnúť pod hladinu koncentrovanejšieho roztoku sacharózy. Výsledkom je pelet, rozdelený na jednotlivé frakcie, podľa hustoty sacharózy.
Precipitácia a dialýza
Proteíny je ďalej často potrebné selektívne vyzrážať − precipitovať z heterogénneho roztoku. Najpoužívanejšou chemikáliou je síran amónny − (NH₄)₂SO₄, ktorý spôsobuje tzv. postupné vysoľovanie (salting-out efekt) proteínov v závislosti od ich rozpustnosti v roztoku s rôznou iónovou silou. Princípom je v podstate „súperenie” síranu amónneho s proteínom o molekuly rozpúšťadla (vody). Precipitovaný proteín tvorí agregáty (cez hydrofóbne interakcie), takže je oddeliteľný od solubilnej fázy centrifugáciou.
Týmto spôsobom je možné, so zvyšujúcou sa koncentráciou síranu amónneho, pozbierať niekoľko frakcií, ktoré obsahujú rôzne proteíny, a analyzovať tieto frakcie na prítomnosť predmetného rekombinantného proteínu (napr. pomocou SDS-PAGE).
Precipitácia proteínov týmto spôsobom nespôsobuje denaturáciu proteínov. Síran amónny je z roztoku odstrániteľný dialýzou. Dialýza roztoku proteínu je metóda na odstránenie nízkomolekulových chemických látok z roztoku, ktoré by mohli negatívne ovplyvňovať ďalšie purifikačné kroky, príp. biologické vlastnosti proteínu. Dialýza prebieha v dialyzačných sáčkoch za stáleho miešania v tlmivom roztoku a pri nízkej teplote (4 °C). Póry dialyzačného sáčku prepúšťajú len malé molekuly, kým nenastane rovnováha medzi zložením obidvoch roztokov. Prostredníctvom dialýzy možno niektoré proteíny renaturovať do biologicky aktívnej konformácie. Dialýzou nemožno odstrániť veľmi nabité molekuly, napr. SDS.
Extrakcia proteínov z tkanív a kultivovaných buniek
Extrakcia proteínov z tkanív a kultivovaných buniek je základným krokom prípravy vzorky, ktorý sa vykonáva počas mnohých biochemických a analytických techník, ako sú ELISA, PAGE, Western blotting, hmotnostná spektrometria alebo purifikácia proteínov.
Regulácia teploty a ultrazvuková homogenizácia
Aby sa zabezpečil vysoký výťažok bielkovín bez tepelnej denaturácie, musí sa počas extrakcie regulovať teplota. Najmodernejšie ultrazvukové homogenizátory Hielscher - tiež nazývaný ultrazvukový dezintegrátor alebo ultrasonizátor - sú presne ovládateľné. Dodávajú sa so zásuvným snímačom teploty. V možnostiach nastavenia ultrazvukového homogenizátora je možné nastaviť maximálnu teplotu.
Na prípravu tkaniva celej veľkosti (napr. obličiek, srdca, pľúc, svalov atď.) by sa tkanivo malo rozpreparovať na veľmi malé kúsky čistými nástrojmi, najlepšie na ľade a čo najrýchlejšie, aby sa zabránilo degradácii proteázami (napr. lyzačný pufer, ako je RIPA, alebo hypotonický lyzačný pufer obsahujúci proteázu a kokteil inhibítorov fosfatázy). Po pitve sa vzorka ponorí do kvapalného dusíka na rýchle zmrazenie. Vzorka sa môže skladovať pri teplote -80 °C na neskoršie použitie alebo sa môže uchovávať na ľade na okamžitú homogenizáciu.
Bezprostredne pred ultrazvukovou extrakciou sa do skúmavky na vzorku rýchlo pridá ľadovo studený lýzny pufer (s inhibítormi proteázy DTT, leupeptínom a aprotinínom) (na ~10 mg tkaniva sa odporúča približne ~ 600 μl pufra). Ultrazvuková homogenizácia, lýza a extrakcia sa vykonáva pomocou ultrazvukového homogenizátora, ako je UP100H alebo UP200Ht, vybaveného sonotródou s mikrohrotom. Trvanie sonikácie je 60-90 sekúnd v režime ultrazvukového cyklu 15 sekúnd sonikácie a 10 sekúnd odpočinku. Po ultrazvukovej homogenizácii / extrakcii sa lyzát odstredí pri 27 000 g po dobu cca. 20 min.
Pre homogénnu zmes séra a fosfátového pufra sa vzorka najskôr víruje pred ultrazvukovou lýzou buniek. Na ultrazvukovú lýzu sa vzorka sonikuje ultrazvukovým laboratórnym homogenizátorom, ako je UP100H, počas 8 cyklov pri 20% amplitúde, pre cykly každých 5 sekúnd zapnutých a 15 sekúnd vypnutých. Extrakcia proteínov sa vykonáva sonikáciou v cykloch (pulzačný režim) a umiestnením vzorky na ľad, aby sa zabránilo prehriatiu a tepelnej degradácii vzorky.

Čerstvé, mäkké rastlinné tkanivo, napr. mach atď., možno ľahko narušiť jednoduchým umiestnením nasekaného vzorkového materiálu do lyzačného pufra na sonikáciu. Tvrdé, ligenózne rastlinné tkanivá, ako sú semená, jedľové ihličie atď., by mali byť mleté nasucho. Niektoré tvrdé drevité rastlinné materiály musia byť pred extrakciou sonikáciou zmrazené a rozomleté v tekutom dusíku. V prípade suspenzií rastlinných bunkových kultúr väčšinou postačuje ultrazvukové ošetrenie medzi 30 a 150 sekundami v lýznom pufri.
Tento návod vysvetľuje, aký typ sonikátora je najlepší pre vaše úlohy prípravy vzoriek, ako je lýza, narušenie buniek, izolácia proteínov, fragmentácia DNA a RNA v laboratóriách, analýza a výskum. Vyberte si ideálny typ sonikátora pre vašu aplikáciu, objem vzorky, počet vzoriek a priepustnosť. Na ultrazvukovú extrakciu proteínu albumínu z jemne mletého prášku z tekvicových semien sa do sklenenej kadičky s objemom 250 ml pridá 10 g odtučneného prášku z tekvicových semien a 100 ml deionizovanej vody ako rozpúšťadlo. Extrakcia proteínu pozostáva z dvoch krokov: Po prvé, vzorka sa sonikuje ultrazvukový ultrazvuk sondového typu UP400St (400W, 24kHz) vybavený sonotródou S24d7. Sklenená kadička sa počas ultrazvukovej homogenizácie umiestni do studeného vodného kúpeľa. Zásuvný snímač teploty a nastavenia regulácie teploty ultrazvuku UP400St zaisťujú, že teplota vzorky je vždy udržiavaná pod 30 °C. Presnou reguláciou teploty počas sonikácie sa zabráni denaturácii albumínu. Po druhé, extrakcia sa vykonávala mixérom pri otáčkach 200 ot./min a pri 30 °C. Potom sa kadička prenesie do termostatickej trepačky.
Globulín sa odstraňuje dialýzou destilovanou vodou. Po odstránení globulínu sa môže odobrať vzorka proteínového extraktu na stanovenie albumínového profilu a následne sa upraví na pI=3,0 s použitím 0,1 M HCl na koaguláciu albumínu. Pevná fáza sa oddelí centrifugáciou pri 5000 g, 20 °C a znovu sa rozpustí v deionizovanej vode.
Na získanie plne funkčného enzýmu iNOS (napr. na skríning liekov) sa odporúča nasledujúci protokol: Bunková suspenzia by sa mala umiestniť na ľad a sonikovať UP100H pri amplitúde 10 μm v cyklickom režime 5 sekúnd sonikácie a 25 sekúnd odpočívať na ľade. Postup by sa mal opakovať cca. 3-krát. Sonikácia môže urýchliť proces solubilizácie bielkovín, ktorý zvyčajne vyžaduje niekoľko hodín. Laboratórne ultrazvuky Hielscher sú výkonné a ľahko ovládateľné. Sú navrhnuté pre prevádzku 24 hodín denne, 7 dní v týždni a sú navrhnuté ako robustné a efektívne laboratórne a stolové zariadenia. Pre všetky zariadenia je možné presne regulovať energetický výkon a amplitúdu. Široká ponuka príslušenstva otvára ďalšie možnosti nastavenia.
Ako funguje ultrazvuk?
Nasledujúca tabuľka poskytuje prehľad našich ultrazvukových prístrojov na prípravu vzoriek, narušenie buniek a extrakciu. Kliknutím na typ zariadenia získate ďalšie informácie o každom ultrazvukovom homogenizátore. V závislosti od vašej aplikácie, materiálu a objemu vzorky vám odporučíme najvhodnejšie nastavenie pre prípravu vzoriek. Kontaktujte nás!
Proteomika a techniky extrakcie
Proteomika je oblasť výskumu, ktorá skúma proteíny a proteóm. Bielkoviny napĺňajú širokú škálu životne dôležitých funkcií v organizmoch. Proteóm je celý súbor proteínov exprimovaných genómom, bunkou, tkanivom alebo organizmom v určitom čase. Proteóm sa mení s časom a odlišnými požiadavkami alebo stresmi, ktorým bunka alebo organizmus podstupuje. Presnejšie povedané, je to súbor exprimovaných proteínov v danom type bunky alebo organizmu v danom čase za definovaných podmienok. Tento termín je zmesou bielkovín a genómu.
Proteíny sú veľké biomolekuly, takzvané makromolekuly - ktoré sú zložené z jedného alebo viacerých dlhých reťazcov aminokyselinových zvyškov. Bielkoviny sú prítomné vo všetkých organizmoch rastlinného aj živočíšneho pôvodu a sú kľúčové pre väčšinu biologických funkcií. Keďže proteíny obsahujú veľa biologických informácií, extrahujú sa na analytické účely, napr. na proteomický výskum. Medzi najdôležitejšie funkcie, ktoré vykonávajú proteíny, patrí katalýza metabolických reakcií, replikácia DNA, reakcia na podnety a transport molekúl z jedného miesta na druhé. Proteíny sa od seba líšia predovšetkým sekvenciou aminokyselín, ktorá je diktovaná nukleotidovou sekvenciou ich génov a ktorá zvyčajne vedie k zloženiu proteínu do špecifickej trojrozmernej štruktúry, ktorá určuje jeho aktivitu. Bielkoviny sú - okrem peptidov - jedna z kľúčových zložiek jedla.
Cloud Point Extraction je predanalytický postup na separáciu a predbežnú koncentráciu analyzovaných látok. V kombinácii s ultrazvukom je možné zintenzívniť extrakciu bodu zákalu, čím sa proces stáva efektívnejším, rýchlejším a šetrnejším k životnému prostrediu. Pri ultrazvuku je extrakcia bodu zákalu podstatne efektívnejšou metódou prípravy analytu.
Gélová elektroforéza je hlavnou metódou separácie a analýzy makromolekúl, ako sú DNA, RNA a proteíny, ako aj ich fragmentov, na základe ich veľkosti a náboja.
Bunková kultúra je kontrolovaný proces rastu, pri ktorom sa bunky kultivujú za kontrolovaných podmienok. Podmienky bunkovej kultúry sa líšia pre každý typ bunky. Vo všeobecnosti prostredie bunkovej kultúry pozostáva z vhodnej nádoby (napr. Petriho misky) so substrátom alebo médiom, ktoré dodáva základné živiny (aminokyseliny, sacharidy, vitamíny, minerály), rastové faktory, hormóny a plyny (CO2, O2) a reguluje fyzikálno-chemické prostredie (pH pufer, osmotický tlak, teplota). Masové kultúry živočíšnych bunkových línií sa používajú pri priemyselnej výrobe vírusových vakcín a iných biotechnologicky odvodených produktov.
Pojem tkanivo opisuje bunkový medziprodukt, kde bunkový materiál je na organizačnej úrovni medzi bunkami a celým orgánom. V tkanive sú zostavené podobné bunky rovnakého pôvodu, ktoré spolu vykonávajú špecifickú funkciu. Vzorky tkaniva sa odoberajú na výskum v biológii, histológii/histopatológii, parazitológii, biochémii, imunohistochémii, ako aj na kultiváciu a extrakciu DNA. Dá sa rozlíšiť medzi živočíšnym (podčlenenie: tkanivo cicavcov) a rastlinným tkanivom. Živočíšne tkanivá sú zoskupené do štyroch základných typov spojivového, svalového, nervového a epiteliálneho tkaniva. Vzorky tkanív sa môžu pripraviť zo živočíšnych alebo rastlinných častí, napr.
Krv, sérum, plazma, mozgovomiechový mok, sliny a synoviálna tekutina sú telesné tekutiny, ktoré sú skvelým zdrojom diagnosticky relevantných informácií. Preto je dôležitá sofistikovaná príprava vzoriek telesných tekutín na analýzu.
Bradfordov test, Lowryho test a test kyseliny bicinchoninovej (BCA) sú bežné testy na stanovenie koncentrácie proteínov.
Lyzačný pufer sa musí zvoliť v súlade s bunkovým materiálom alebo tkanivom (tkanivová kultúra, rastlina, baktérie, huby atď.) a podľa toho, či sú bunky v štruktúre a typu štruktúry. Široká škála lýznych pufrov na extrakciu bielkovín, membrán a organel je formulovaná s jedným alebo viacerými detergentmi. Prací prostriedok sa zvyčajne vyberá prostredníctvom testov pokus-omyl alebo - ak je k dispozícii - podľa existujúceho protokolu extrakcie bielkovín. Prací prostriedok musí byť kompatibilný so zdrojom tkaniva a bielkovinami. Vo všeobecnosti sa najjemnejší prací prostriedok, ktorý funguje na konkrétne tkanivo / proteín, vyberá tak, aby sa zachovala maximálna funkčnosť extraktu. Okrem toho v prípade extrakcie membrán a organel udržuje jemný čistiaci prostriedok membránu neporušenú. Bežne používané čistiace prostriedky v lýznych pufroch sú väčšinou neiónové alebo zwitterionové, napr.
Tkanivá ako mozog, pečeň, črevá, obličky, slezina atď. môžu byť jednoducho pufrované pomocou RIPA - mali by sa však zahrnúť inhibítory proteázy a DTT (napr.
tags: #izolacia #heterogenneho #proteinu